
کبالت (II) کلرید یکی از رایج ترین اشکال کلریدی است که امروزه در آزمایشگاه یافت می شود. فرمول شیمیایی آن CoCl2 و وزن مولکولی آن 129.833 گرم در مول است. این ترکیب غالباً به صورت کلرید هگزاهیدرات کبالت (II) یا کلرید بی آب کبالت (II) عرضه می شود. از کلرید کبالت (CoCl2) برای تولید ویتامین B12 استفاده می شود. همچنین از آن به عنوان رنگ دانه استفاده می شود. این ماده همچنین در ساخت روان کننده های جامد، به عنوان افزودنی برای کودها، به عنوان یک واکنش شیمیایی در آزمایشگاه ها و به عنوان جاذب ماسک های گاز، و آبکاری استفاده می شود.
کلرید کبالت II
کلرید کبالت II | خرید کلرید کبالت II | فروش کلرید کبالت II | قیمت کلرید کبالت II | خرید | فروش

این ماده یک ترکیب غیر آلی از کبالت و کلر، با فرمول CoCl است. این ماده چندین فرم هیدراته (۱،۶،۹،۲) ایجاد می کند.این ماده به رنگ های دی هیدرات بنفش و هگزاهیدرات صورتی است. معمولاً به عنوان کبالت کلرید هگزاهیدرات عرضه می شود.به دلیل سهولت واکنش هیدراتاسیون / کمبود آب و تغییر رنگ حاصل از آن، از کلرید کبالت به عنوان شاخص آب خشک کن استفاده می شود.
رنگ کلرید کبالت تغییر می کند زیرا نمک موجود در محلول به یون ها تفکیک می شود. یون های کبالت در محلول هیدراته شده و رنگ صورتی دارند. افزودن اسید کلریدریک غلیظ به محلول، رنگ محلول را به بنفش مایل به آبی تغییر می دهد. این بدان دلیل است که یون های کلر آب را از مجتمع آب کبالت خارج می کنند.
روش تولید کبالت(II) کلرید
این ماده با عملکرد فلز کبالت یا اکسید، هیدروکسید یا کربنات آن با اسید کلریدریک تهیه می شود:
Co (OH) ۲ + ۲HCl → CoCl۲ + ۲H۲O
محلول موجود، بلورهای هگزاهیدرات را تشکیل می دهد که در اثر حرارت دادن با SOCl۲ به این ماده بی آب تبدیل می شود.متناوباً، هگزاهیدرات ممکن است در اثر کم آبی در جریان کلرید هیدروژن به CoCl۲ بدون آب تبدیل شده و در خلا در دمای ۱۰۰-۱۵۰ درجه سانتی گراد خشک شود.ترکیب بی آب نیز ممکن است با عبور کلر از پودر کبالت بدست آید.
این ماده یک اسید لوئیس ضعیف است. این ماده همچنین یک ترکیب متوسط قدرتمند است که پیش ماده مشترک سایر ترکیبات کبالت است. به راحتی اکسید می شود و اغلب در حضور کاتالیزور استفاده می شود. این ماده یک پیش ماده ضروری برای کبالتوسن و تترالیکل است. گفته می شود کلرید کبالت (II) از نظر سینتیکی بی اثر است.
کاربرد های کبالت(II) کلرید
این ماده به عنوان یک تثبیت کننده کف در آبجو، با جوهر نامرئی برای نقاشی روی شیشه در آبکاری و یک کاتالیزور در واکنشهای گریگنارد، باعث ایجاد اتصال با یک هالید آلی می شود. همچنین برای تهیه چندین نمک کبالت دیگر نیز استفاده می شود. در ساخت ویتامین B12 مصنوعی نیز از این ماده استفاده می شود. حتی اگر این ترکیب باعث آسیب به گلبول های قرمز خون شود.
کلرید کبالت در پاسخ به رطوبت تغییر رنگ می دهد، از این رو اختلاف رنگ بین فرم های بی آب و هگزاهیدرات آن وجود دارد. این ماده اغلب به عنوان شاخصی برای خشک کن های آب استفاده می شود.
از نظر تجاری، از این ماده اغلب برای ساخت درزگیر، چسب استفاده می شود. همچنین از آن برای آبکاری، به ویژه برای آبکاری اشیا با فلز کبالت استفاده می شود. فلز تصفیه سطح نیز یکی دیگر از کاربردهای رایج صنعتی این ترکیب است.
هگزاهیدرات کلرید کبالت می تواند به عنوان القا کننده تولید HIF-1 مورد استفاده برای مطالعه اثرات آپوپتوتیک در سلولهای HepG2 قرار گیرد. کبالت (II) کلرید به عنوان استاندارد رنگی APHA استفاده می شود.
خصوصیات کبالت (II) کلرید
این ماده به صورت دهیدراته، با کریستال های آبی نمایان می شود. فرم دی هیدراته آن آبی بنفش و فرم هگزاهیدرات آن به صورت بلورهای قرمز وجود دارند.این ماده در آب حل می شود.
|
۷۲۴ °C(lit.)
|
Melting point
|
|
۱۰۴۹ °C
|
Boiling point
|
|
۳.۳۵
|
Density
|
|
۴۰ mm Hg ( 0 °C)
|
Vapor pressure
|
|
۵۰۰°C
|
Flash point
|
|
۲-۸°C
|
Storage temp
|
|
۵۸۵.۹g/l soluble
|
Solubility
|
|
beads
|
Form
|
|
Pale blue
|
Color |
|
۳.۳۵۶
|
Specific Gravity
|
|
soluble
|
Water Solubility
|
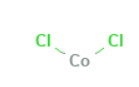 |
Structure |
 |
Chemical Safety |
| CoCl۲ Or Cl۲Co | Molecular Formula |
|
۷۶۴۶-۷۹-۹Cobaltchloride Cobalt chloride (CoCl2) MFCD00010938 cobalt(II)chloride |
Synonyms |
| ۱۲۹.۸۴ g/mol | Molecular Weight |
نکاتی درمورد کبالت (II) کلرید
این ماده بسیاری از واکنش های تجزیه دوگانه را در محلول آبی ایجاد می کند تا رسوبات نمک های کبالت نامحلول ایجاد کند. به عنوان مثال، گرم کردن محلول آن با کربنات سدیم باعث تولید کربنات کبالت (II) می شود:
CoCl۲ + Na۲CO۳ CoCO۳ + ۲NaCl
واکنش با هیدروکسید قلیایی، هیدروکسید کبالت (II) تولید می کند:
CoCl۲ + ۲NaOH → Co (OH) ۲ + ۲NaCl
واکنش با فسفات هیدروژن آمونیوم باعث تولید فسفات کبالت (II) می شود:
۳CoCl۲ + ۲ (NH۴) ۲HPO۴ → Co۳ (PO۴) ۲ + ۴NH۴Cl + 2HCl
در حالی که فلوراید کبالت (II) محصول واکنش کلرید کبالت بی آب (II) با اسید هیدروفلوئوریک است، فلوراید کبالت (III) از فلوراسیون محلول آبی این ماده بدست می آید.
با افزودن نیتریت پتاسیم به محلول کلرید کبالت (II)، هگزانیتروکوبالتات پتاسیم بلورین زرد (III) ، K۳Co (NO۲) ۶ تولید می شود.این ترکیب در دوزهای بالا سمی است. علائم مسمومیت با این ماده شامل درد قفسه سینه، گرگرفتگی جلدی، حالت تهوع، استفراغ، ناشنوایی عصب و نارسایی احتقانی قلب است. اثرات سیستمیک ناشی از بلع در انسان شامل بی اشتهایی ، افزایش اندازه تیروئید و کاهش وزن است.
منابع :
https://www.ebi.ac.uk/chebi/searchId.do?chebiId=35696
https://www.americanelements.com/cobalt-ii-chloride-hydrate-69098-14-2
https://www.chemicalbook.com/ChemicalProductProperty_EN_CB7226636.htm
https://www.chemicalbook.com/ChemicalProductProperty_EN_CB8226062.htm
https://melscience.com/US-en/articles/cobalt-colors-experiment/
https://pubchem.ncbi.nlm.nih.gov/compound/Cobalt-chloride-hexahydrate
 شرکت اوج آزما پلاست در سال 1392 در ایران تاسیس گردید. هدف اصلی همکاران ما کوشش در جهت بالابردن سطح سلامت در جامعه جهانی است. شرکت اوج آزما پلاست در زمینه واردات و تولیدات تجهیزات و ملزومات آزمایشگاهی و بیمارستانی فعالیت داشته و از ابتدای شروع فعالیت همواره
شرکت اوج آزما پلاست در سال 1392 در ایران تاسیس گردید. هدف اصلی همکاران ما کوشش در جهت بالابردن سطح سلامت در جامعه جهانی است. شرکت اوج آزما پلاست در زمینه واردات و تولیدات تجهیزات و ملزومات آزمایشگاهی و بیمارستانی فعالیت داشته و از ابتدای شروع فعالیت همواره